癌癥作為全球死亡的主要原因之一,根據美國癌癥協會的數據,癌癥仍然是美國死亡的第二大殺手,在2022年導致近600萬人死亡。在過去的幾十年里,科學家和醫療專業人員一直在積極開展癌癥研究,尋求新的治療手段和預防措施。包括但不限于手術、化療、放療、靶向治療、基因治療和免疫治療。而放射性配體療法(Radioligand therapy, RLT)作為一種新型治療手段,近年來在癌癥的診斷、治療和監測方面展現出了顯著的發展勢頭。作為晚期癌癥患者的一種精準核醫學治療形式,RLT利用具有放射性的靶向藥物,即放射性配體,特異性結合癌細胞上所表達的受體,再以直接和精確的方式通過射線殺死癌細胞,同時保留周圍的健康組織。RLT的一個成功例子是Pluvicto(177Lu-PMSA-617),它是2022年被批準的第一個前列腺特異性膜抗原靶向的放射性配體療法,在前列腺癌患者中展現了顯著的臨床療效。
放射性配體由四個部分組成:放射性同位素、靶向配體、連接子和螯合劑。高能放射性同位素,如α和β發射體,提供導致DNA損傷的輻射,通常用于癌癥治療,另一方面,γ射線因其能量非常微弱,但穿透能力強的特點適合用于開發SPECT(單光子發射計算機斷層成像)與PET(正電子發射斷層成像)用放射性診斷藥物。放射性同位素與螯合劑形成的金屬螯合物通過小分子連接子與靶向配體連接,而DOTA(1,4,7,10-四氮雜環十二烷-1,4,7,10-四乙酸)因其對許多放射性同位素具有高親和力和穩定性而被廣泛用作螯合劑。
在核藥臨床前開發中,研究人員往往使用冷藥(放射性治療藥物的非放射性或衰變形式,例如,175Lu)作為熱藥(具有放射性,例如177Lu)替代物,在相對低的劑量水平下研究RLT候選藥物的安全性。臨床前安全性研究中使用的供試品包含冷藥(放射性治療藥物的非放射性或衰變形式,即ligand-linker-chelator with nonradioactive metal)和游離配體(即ligand-linker-chelator without metal)。在文獻“LC?MS/MS Bioanalysis of Radioligand Therapeutic Drug Candidate for Preclinical Toxicokinetic Assessment”的報道中,諾華的研究人員開發了一種高選擇性和高靈敏度的旨在檢測動物血漿樣品中游離配體(NVS001)和冷藥(175Lu-NVS001)的LC?MS/MS方法。

一般來說,具有螯合結構的化合物在液相分析往往容易與儀器不銹鋼管路或者色譜柱不銹鋼管壁發生作用,導致峰形異常、靈敏度下降或重現性欠佳等問題,除此以外,多肽也容易與樣品容器或者內源性蛋白發生非特異性吸附。因而文獻中所提到的分析挑戰有:
未鰲合配體藥物NVS001靈敏度差
未鰲合配體藥物NVS001易與內源性金屬離子如鉀形成復合物
66Ga標記的內標在樣品提取和分析過程中出現66Ga離子流失
待測物在低濃度不穩定
血樣提取樣品中內標響應不一致
EDTA在液相分析中作為流動相添加劑中的一種,往往用作類似金屬屏蔽劑的作用,來改善具有螯合結構的化合物峰形和靈敏度問題,在該研究中,我們不僅可以看到在流動相中做了類似的添加,而且在樣品的前處理過程中同樣使用到了EDTA。
色譜柱:C18, 100 × 2.1 mm 1.8 μm
流動相A:40 mM碳酸氫銨水溶液(含20 µM EDTA和0.04%氨水)
流動相B:甲醇
柱溫:40℃
流速:0.6 mL/min
進樣體積:10~20 µL (EDTA和氨水添加到乙腈/甲醇 (50:50, V/V)洗針液以減少殘留)
檢測器:LC?MS/MS 正離子模式
NVS001: m/z 443.9 → 292.3
175Lu-NVS001: 529.9 → 421.3
66Ga-NVS001: 476.9 → 368.3

NVS001和175Lu-NVS001 (0.2 mg/mL) 儲備液配置:乙腈/DMSO (30/70, V/V),用甲醇/水 (50/50, V/V, 含0.1%甲酸和10 µM EDTA )作稀釋劑配置0.01~5 µg/mL溶液
66Ga-NVS001內標工作液 (15 ng/mL) :將內標儲備液 (0.1mg/mL)用甲醇/水 (50/50, V/V, 含0.1%甲酸和10 µM EDTA )稀釋配置
上述所有溶液均置于PP管中于2-8℃保存
校準曲線和QC樣品配置:將適量濃度為0.01~5 µg/mL的NVS001和175Lu-NVS001標液與1%磷酸處理的血漿樣品按1:24 (V/V) 分別配置成0.500, 1.00, 3.00, 10.0, 25.0, 100, 200, 250 ng/mL的校準曲線樣品;QC樣品濃度分別為0.500, 1.50, 10.0, 100, 190 ng/mL;所有QC樣置于PP小瓶中≤?70 °C保存
所有校準標樣,QC樣和待測樣品均置于低溫(wet ice)中解凍和處理
向96孔板中分別加入25 µL空白血漿,校準標樣,QC樣和待測樣品;再向除基質空白樣以外的所有孔中加入25 µL 66Ga-NVS001內標工作液 (15 ng/mL) ;基質空白樣則加入25 µL甲醇/水 (50/50, V/V, 含0.1%甲酸和10 µM EDTA )
向所有孔中加入300 µL蛋白沉淀試劑 (25:25:50 [V/V/V], 丙酮/乙腈/甲醇含0.2%甲酸和20 µM Na2EDTA ,渦旋10min后1640×g 離心5min
取300 µL上清液轉移至含10 µL 異丙醇/丙二醇 (50:50 [V/V]),渦旋后于30℃下氮吹至盡干,最后用150 µL甲醇/水 (25:75 (V/V) 含0.1%甲酸和10 µM Na2EDTA),渦旋10min后進樣分析
沉淀試劑優化過程:
純乙腈作為沉淀試劑無法獲得良好的NVS001 和 175Lu-NVS001回收率
替換為純甲醇可實現理想的回收率,但同時帶來基線背景升高和干擾峰的問題
Na2EDTA和甲酸的加入可有效防止內標工作液中66Ga的丟失
犬血樣品提取后內標響應偏差較大(大鼠血樣表現正常),經過優化,25%丙酮的加入和至少10min的蛋白沉淀渦旋有助于確保內標響應的一致性;同時,將Na2EDTA和甲酸的添加濃度由10 µM和0.1%分別增加至20 µM和0.2%有助于消除由上述操作帶來的內標66Ga流失的問題

NVS001: m/z 443.9 → 292.3進溶劑標樣或者血漿提取樣品響應都不及預期,進一步考察顯示,NVS001易與鉀離子形成復合物 (K-NVS001, m/z 462.9 → 310.3 );中濃度QC提取樣品,含NVS001和175Lu-NVS001各100 ng/mL,流動相未添加20 µM Na2EDTA可觀察到明顯的K-NVS001峰,175Lu-NVS001和66Ga-NVS001的響應并未受到添加Na2EDTA的影響(Figure 2)。

通常DOTA和大多數三價金屬離子如GaIII and LuIII的配合物在室溫下是穩定的,但是在以下情形易出現金屬離子的丟失:
與內源性金屬離子發生交換
堿性條件下易形成氫氧化物 (即 [Ga(OH)4]? )
面臨問題
通過考察NVS001在溶劑標樣和175Lu-NVS001加標血樣 (250ng/mL) 的響應,并未發現175Lu-NVS001向NVS001的轉化,表明Lu-DOTA配合物穩定性良好
對只含66Ga-NVS001加標的空白血樣采用甲醇/乙腈 (50:50, V/V) 提取分析,觀察到明顯的NVS001峰(如Figure S-1-A所示);然而對于只含66Ga-NVS001的溶劑標樣,即使采用相同的提取步驟,卻并未觀察到該現象,表明66Ga流失更大可能是由于基質中存在的金屬離子
解決方案
向內標工作液和蛋白沉淀試劑加入10 µM Na2EDTA,同時加入0.1%甲酸以避免66Ga的氫氧化物形成,如Figure S-1-B所示,66Ga-NVS001加標的空白血樣提取后分析可觀察到NVS001峰響應出現10倍降低,但是,其峰面積仍高于對應LLOQ的20%
進一步優化:
1)小體積異丙醇/丙二醇 (50:50 [V/V])加入到蛋白沉淀后的上清液以避免吹干;
2)將氮吹溫度從40℃降至30℃。經過優化,如Figure S-1-C所示,NVS001峰未再檢出
簡而言之,EDTA不僅在LC-MS/MS流動相,而且在樣品前處理鰲合基質和系統中的游離金屬離子方面發揮重要作用;同時,維持酸性環境體系和優化氮吹條件,都對在樣品提取過程中消除內標 66Ga-NVS001中Ga的流失具有重要意義。
分別考察冰袋保存的QC樣本低濃度(1.5 ng/mL) 和高濃度(190 ng/mL) NVS001 and 175Lu-NVS001的24h穩定性
低濃度(1.5 ng/mL) QC樣本在冰袋保存24h后分析, NVS001 和 175Lu-NVS001在大鼠血漿和犬血漿的回收率分別只有8%和20%,低濃度(190 ng/mL) 并未觀察到此現象,同時,校準曲線藥品低濃度也出現偏低而影響線性的情況
由于多肽部分和進樣小瓶及96孔板的非特異性吸附,或者與生物基質中內源性蛋白的結合,從而在樣品轉移和蛋白沉淀過程中出現待測物的損失
然而,低吸附進樣小瓶和96孔板的使用并未改善低濃度樣品的回收率問題
進一步考察樣品管轉移的影響:將含NVS001 和 175Lu-NVS001各4 ng/mL的樣品依次在樣品管間轉移,每次轉移前先渦旋1min,然后在冰袋保存5min以保證吸附,LC-MS/MS分析結果如Figure S-2所示,未有明顯非特異性吸附
樣品和內源性組分的吸附干擾考察:低濃度QC樣本分別用抗壞血酸、磷酸和乳酸處理,然后置于冰袋和室溫環境下24h,結果顯示,抗壞血酸處理回收率(30-60%),磷酸或乳酸處理回收率(80-100%)。綜合評估,血漿樣本采用20%磷酸溶液按20:1(V/V)進行處理

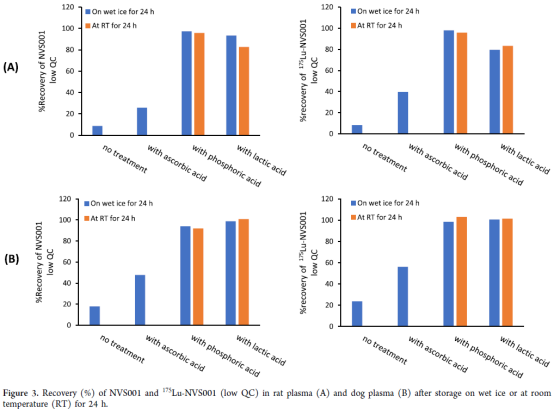
從文獻所報道的整個方法開發過程可以看到,該LC-MS/MS生物分析方法具有高選擇性和高靈敏度的優點,能夠基于25μL樣品體積的條件下在0.5-250ng/mL濃度范圍內用于同時測定大鼠和犬血漿中的游離配體(NVS001)和冷藥(175Lu-NVS001)。同時表明向流動相中添加螯合劑EDTA可以顯著提高游離配體NVS001的靈敏度,同時最大限度避免了NVS001與樣品基質中的金屬離子(例如K)形成螯合物影響分析結果。另外,向包括內標工作液、蛋白沉淀劑和復溶液在內的眾多溶劑中引入EDTA和甲酸有助于最大限度地減少樣品提取過程中內標66Ga的流失;同時采取相對溫和的氮吹條件可進一步避免66Ga的流失。而用1%磷酸預處理血漿樣品則能有效防止低濃度下待測物與內源性蛋白質結合而導致的結果“不穩定性”發生。此外,在蛋白沉淀劑中加入一定體積的丙酮也有助于獲得一致的內標響應。更多的研究也表明,該LC-MS/MS工作分析流可擴展至其他放射性配體藥物在生物樣品中的的定量分析,從而支持臨床前RLT藥物的開發。
站在不同的視角來看,除了從所使用的溶劑和流動相中添加EDTA來避免上述文獻中所遇到的分析問題,惰性的儀器管路以及惰性的色譜柱柱管及篩板(例如鈦合金材質)是不是可以從另外一個維度來優化和解決這類問題呢,再延展到具有放射性的熱藥的分析,普通的不銹鋼色譜柱和鈦合金材質的色譜柱在進樣具有放射性的藥物的分析過程中,柱管內表面是否會發生不一樣的變化,繼而影響到峰形、回收率等分析結果呢,相信隨著更多關于放射性核素偶聯藥物的研究進展,我們對于核藥色譜分析所遇到的難題會逐漸解開。
關于鈦合金材質色譜柱



LC?MS/MS Bioanalysis of Radioligand Therapeutic Drug Candidate for Preclinical Toxicokinetic Assessment. Anal. Chem. 2023, 95, 10812?10819.
相關產品
免責聲明
- 凡本網注明“來源:化工儀器網”的所有作品,均為浙江興旺寶明通網絡有限公司-化工儀器網合法擁有版權或有權使用的作品,未經本網授權不得轉載、摘編或利用其它方式使用上述作品。已經本網授權使用作品的,應在授權范圍內使用,并注明“來源:化工儀器網”。違反上述聲明者,本網將追究其相關法律責任。
- 本網轉載并注明自其他來源(非化工儀器網)的作品,目的在于傳遞更多信息,并不代表本網贊同其觀點和對其真實性負責,不承擔此類作品侵權行為的直接責任及連帶責任。其他媒體、網站或個人從本網轉載時,必須保留本網注明的作品第一來源,并自負版權等法律責任。
- 如涉及作品內容、版權等問題,請在作品發表之日起一周內與本網聯系,否則視為放棄相關權利。
 手機版
手機版 化工儀器網手機版
化工儀器網手機版
 化工儀器網小程序
化工儀器網小程序
 官方微信
官方微信 公眾號:chem17
公眾號:chem17
 掃碼關注視頻號
掃碼關注視頻號



















 采購中心
采購中心